
Taula de continguts:
- Autora Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Última modificació 2025-01-22 16:56.
La depressió del punt de congelació és una propietat col·ligativa observada en solucions que resulta de la introducció de molècules de solut a un dissolvent. Els punts de congelació de les solucions són tots inferiors als del dissolvent pur i són directament proporcionals a la molalitat del solut.
En conseqüència, com es calcula la molalitat a partir de la depressió del punt de congelació?
Estratègia:
- Pas 1: calculeu la depressió del punt de congelació del benzè. Tf = (Punt de congelació del dissolvent pur) - (Punt de congelació de la solució)
- Pas 2: Calcula la concentració molal de la solució. molalitat = mols de solut / kg de dissolvent.
- Pas 3: calculeu Kf de la solució. Tf = (Kf) (m)
De la mateixa manera, per què s'utilitza Molality en el punt de congelació? Wendy K. Les propietats col·ligatives són propietats físiques de les solucions, com l'ebullició punt elevació i Punt de congelació depressió. Per això fem servir molalitat (mols de solut per kg de dissolvent) ja que el kg de dissolvent no canvia amb temperatura.
També la pregunta és, què vols dir amb depressió del punt de congelació?
Depressió del punt de congelació es produeix quan el Punt de congelació d'un líquid es baixa o deprimit afegint-hi un altre compost. La solució té un menor Punt de congelació que el del dissolvent pur.
Com afecta la molality al punt d'ebullició?
Com més gran sigui la concentració ( molalitat ), més alt és punt d'ebullició . Pots pensar en això efecte com a solut dissolt que elimina les molècules de dissolvent a la superfície, on bullint es produeix. Per tant, requereix una superior temperatura perquè s'escapin prou molècules de dissolvent per continuar bullint a pressió atmosfèrica.
Recomanat:
Quina és la relació matemàtica entre la resistència actual i l'aparell de tensió?
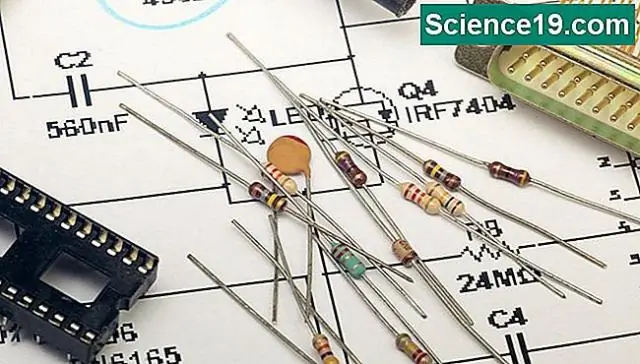
Llei d'Ohm. La relació entre tensió, corrent i resistència es descriu per la llei d'Ohm. Aquesta equació, i = v/r, ens diu que el corrent, i, que circula per un circuit és directament proporcional a la tensió, v, i inversament proporcional a la resistència, r
Com es troba la massa molar des del punt de congelació?

Pas 1: enumera les quantitats conegudes i planifica el problema. Utilitzeu la depressió del punt d'alliberament egin{align*}(Delta T_f)end{align*} per calcular la molalitat de la solució. A continuació, utilitzeu l'equació de molalitat per calcular els mols de solut. A continuació, dividiu els grams de solut pels mols per determinar la massa molar
Com es determina el punt de congelació?
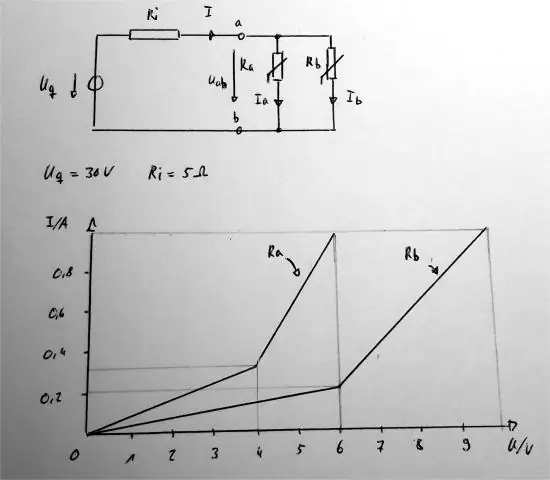
Estratègia: Pas 1: Calcula la depressió del punt de congelació del benzè. Tf = (Punt de congelació del dissolvent pur) - (Punt de congelació de la solució) Pas 2: Calcula la concentració molal de la solució. molalitat = mols de solut / kg de dissolvent. Pas 3: Calculeu Kf de la solució. Tf = (Kf) (m)
Com afecta la depressió del punt de congelació el pes molecular?

Així, a mesura que augmenta la massa molar, la depressió del punt de congelació disminueix. És a dir, augmentar la massa molar (o molecular) tindrà un efecte menor sobre el punt de congelació
Què és el punt de fusió d'ebullició i de congelació?

Quan un sòlid es converteix en líquid s'anomena fusió. El punt de fusió de l'aigua és de 0 graus C (32 graus F). Quan passa el contrari i un líquid es converteix en sòlid, s'anomena congelació. Ebullició i condensació. Quan un líquid es converteix en gas s'anomena ebullició o vaporització
