
- Autora Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- Última modificació 2025-01-22 16:56.
A talp de CuSO4•5H2O conté 5 talps d'aigua (que correspon a 90 grams d'aigua) com a part de la seva estructura. Per tant, la substància CuSO4•5H2O consta sempre d'un 90/250 o un 36% d'aigua en pes.
De la mateixa manera, us podeu preguntar, com trobeu el percentatge en massa d'aigua en un hidrat?
Divideix el massa del aigua perdut per la massa de hidratar i multiplicar per 100. El teòric (real) per cent hidratació ( per cent d'aigua ) pot ser calculada des del fórmula del hidratar dividint el massa de aigua en un talp del hidratar pel molar massa del hidratar i multiplicant per 100.
Posteriorment, la pregunta és, quina és la massa de CuSO4 5h2o? 159,609 g/mol
Respecte a això, quin és el percentatge en massa d'aigua del sulfat de coure II hidrat?
159.62 / 249.72 * 100 = 63.92 per cent . Això vol dir que una mostra de 100 grams sulfat de coure pentahidrat contindrà 63,92 grams de sulfat de coure . També vol dir que sulfat de coure pentahidratat conté 100 - 63,92 = 36,08 per cent d'aigua per massa.
Per què el CuSO4 5h2o es considera un hidrat?
El motiu que CuSO4 . 5H20 és considerat un "hidratat ".", o més exactament un "pentahidrat" és degut a aquestes molècules d'aigua que s'integren als cristalls del hidratat forma.
Recomanat:
Quin percentatge de la superfície terrestre està cobert per aigua?
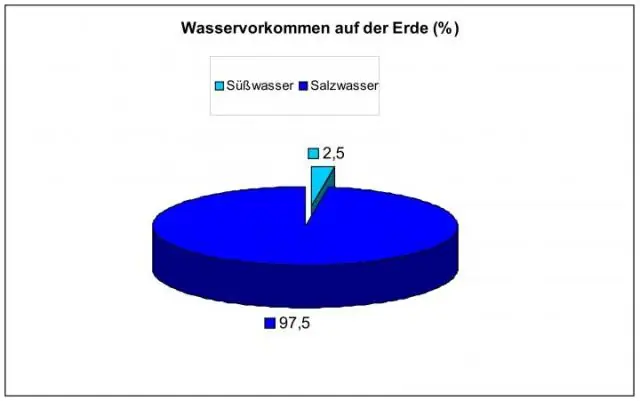
71 per cent
Quin és el percentatge en massa d'oxigen del sulfat de potassi?

Composició percentual per element Element Símbol Percentatge en massa Oxigen O 36,726% Sofre S 18,401% Potassi K 44,874%
Quin percentatge de l'aigua de la Terra es pot trobar al sòl?

La terra té una gran quantitat d'aigua, però, malauradament, només un petit percentatge (al voltant del 0,3%) és fins i tot utilitzable pels humans. L'altre 99,7 per cent es troba als oceans, sòls, casquets glacials i flotant a l'atmosfera. Tot i així, gran part del 0,3 per cent que es pot utilitzar és inassolible
Quin és el percentatge en massa de Na en NaF?

Composició percentual per element Element Símbol Percentatge en massa Sodi Na 54,753% Fluor F 45,247%
Quanta aigua hi ha a l'hidrat?

MESURA EXPERIMENTAL DEL PERCENT D'HIDRATACIÓN: La diferència entre les dues masses és la massa d'aigua perduda. Dividir la massa de l'aigua perduda per la massa original d'hidrat utilitzat és igual a la fracció d'aigua del compost. Multiplicant aquesta fracció per 100 s'obté el percentatge d'aigua de l'hidrat
